 �@
�@ �@
�@
�@���V���̌o�H
�@�y�|�C���g�z
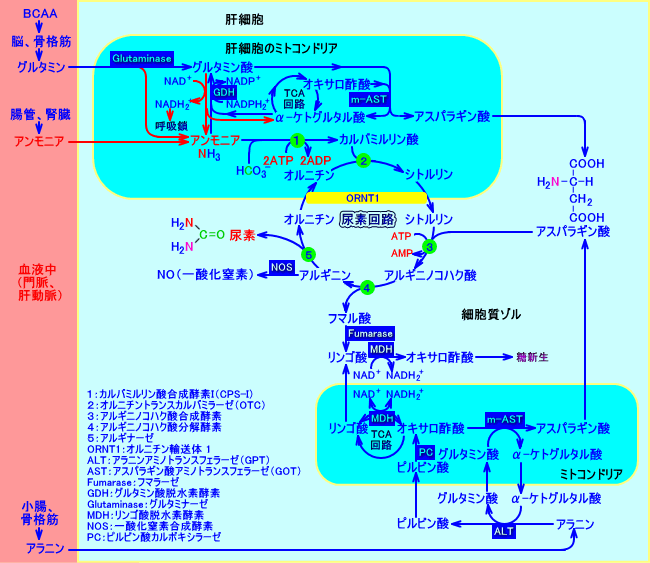
�@�̑��́A��H�����ɁA���V���ɂ��A�A�~�m�_������A�u�h�E�������o���āA���t���ɋ�������B��H���ɂ́A�A�~�m�_�i�A���j���A�A�X�p���M���_���j�A���_�A�O���Z���[�����A���V���̒Y�f���ɂȂ�B
�@���V���i�זE�����j����̂ɕK�v�ȃG�l���M�[�iNADH2+���j�́A���b�_����-�_���i�~�g�R���h���A���j���邱�Ɠ��ɂ���āA�����i�����j�����B���b�_�́A�̓��ł́A���ɕϊ��o���Ȃ����A���b�_�̃G�l���M�[�́A���V���ɗ��p�����B
�@���b�_�̃�-�_���Ɉُ킪����ƁiFAOD���j�A���V������Q����A��H�����ɁA��P�g�����ጌ���𗈂����B
�@�̑��ł́A��H�������V�����s����ۂɂ́A�����S�_�A���n�i�����S�_-��-�P�g�O���^���_�A���́j�ɂ��A���V���ɕK�v��NADH2+���A�~�g�R���h�����i�}�g���b�N�X�j����A�~�g�R���h���A�O�i�זE���]���j�ɁA�A������B
�@���V���̌o�H���̑��ɑ��݂��邱�Ƃɂ��A�̑��ŁA���b�_����-�_�����ē���ꂽ�G�l���M�[���A�O���R�[�X�Ƃ��Ē~�ς��A���̑g�D�ŁA���p���邱�Ƃ��o����B
�@��H�����ɂ́A�]�ɕK�v�Ȍ������ێ����邽�߂ɁA�̑��ŁA�u�h�E���i�O���R�[�X�j���A�A�~�m�_�i�������A�~�m�_�F���P�j�̒Y�f���i�A�s���r���_�A���_�i���Q�j�ATCA��H�̒��ԑ́A�������b�̉��������Ő���������O���Z���[���i�O���Z�����j������A���V���igluconeogenesis�j����܂��B
�@�A�~�m�_�i�������A�~�m�_�j�̒Y�f���i�A�s���r���_�A���_�ATCA��H�̒��ԑ̂́A�I�L�T���|�_���o�R���āA���V���ɗ��p����܂��B
�@���ɂ́A�����l�i�����̃O���R�[�X�Z�x�j�́A�O���R�[�Q�������iglycogenolysis�j�ƁA���V���igluconeogenesis�j�Ƃɂ���Ĉێ�����܂��B
�@���V���́A��Ɋ̑��ōs���܂��B���V���́A�ꕔ�A�t���ł��s���܂��B�Q���Ԃ��i�s����ƁA�t���ł̓��V�����A�d�v�ɂȂ�܂��B
�@���V����90%�́A�A�~�m�_�i�������A�~�m�_�j�̒Y�f���i���A���p����܂��B���V����10%�́A�O���Z���[���i���b�g�D���g���O���Z���h���������ꐶ�������j�A���_�A�s���r���_�i�ؓ��ŃA���j���ɕϊ�����̑��ɗA�������j�̒Y�f���i�����p����܂��B
�@���b�_�́A��-�_���ɂ��A�A�Z�`��-CoA�ɕ�������܂��B
�@�����̑̂ɂ́A�A�Z�`��-CoA���A�I�L�T���|�_�ɕϊ������ӌo�H�i�y�f�j�́A����܂���B
�@�]���āA���b�́A�u�h�E���i�O���R�[�X�j�ɕϊ�����܂���B
�@���̂悤�ȓ��V���igluconeogenesis�j�́A��Ɋ̑��ōs���܂��B
�@�C���X�����́A�̑��ł̓��V�����A�}�����܂��B
�@�̑��́A�����Ԃ��H�����ɂ́A���V���ɂ��̐Ö����猌���Ƀu�h�E�����������A�H����ێ悵�Ė喬���o�ău�h�E������������ƁA�喬������u�h�E������荞�݁A�̐Ö��ւ̃u�h�E���������~���܂��B
�@���V���̌o�H�́A���̋t�o�H�ł͂���܂���B
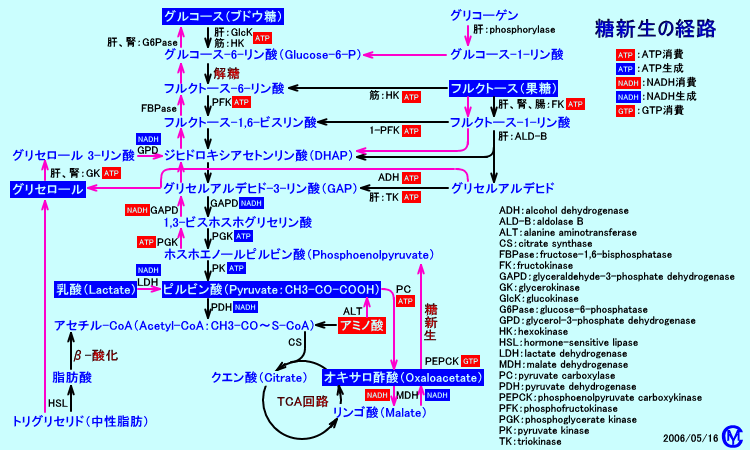
�@�s���r���_���O���R�[�X�܂����V���igluconeogenesis�j����ۂɁA��t�I�Ȓi�K��G�}����̂́A���L�̂S�̍y�f�ł��B
�@�P�D�s���r���_�J���{�L�V���[�[�ipyruvate carboxylase�j
�@�s���r���_�J���{�L�V���[�[�́A�~�g�R���h���A���ŁA�s���r���_���A�I�L�T���|�_�ɕϊ�����y�f�B
�@���b�_����-�_������Đ�����A�Z�`��-CoA�́A�O���R�[�X�ɕϊ�����܂��A�A�Z�`��-CoA�ɂ��A�s���r���_�J���{�L�V���[�[���A����������܂��i�s���r���_�L�i�[�[�̉I��H�j�B

�@�Q�DMDH�i�����S�_�E���f�y�f�Fmalate dehydrogenase�j
�@�~�g�R���h���A���� �I�L�T���|�_�́A�~�g�R���h���A������ʉߏo���Ȃ��̂ŁA��U�AMDH�ɂ��A�����S�_�ɂȂ��āA�����S�_-�A�X�p���M���_�V���g���ɂ��A�~�g�R���h���A������ʉ߂��āA�~�g�R���h���A�O�i�זE���]���j�Ɉڍs���A�Ă�MDH�ɂ��A�I�L�T���|�_�ɖ߂�܂� �i�s���r���_�L�i�[�[�̉I��H�j�B
�@�R�DPEPCK�iphosphoenolpyruvate carboxykinase�j
�@PEPCK�i�z�X�z�G�m�[���s���r���_�J���{�L�V�L�i�[�[�j�́A�זE���]���ŁA�I�L�T���|�_���A�z�X�z�G�m�[���s���r���_�iPEP�j�ɕϊ�����y�f�i�s���r���_�L�i�[�[�̉I��H�j�B
�@�Ȃ��A�q�g�ł́APEPCK�́A�~�g�R���h���A���ɂ����݂��A�������ꂽPEP�́A�~�g�R���h���A����ʉ߂��āA�זE���]���ɗA������܂��i���R�j�B
�@�S�D�t���N�g�[�X-1,6-�r�X�z�X�t�@�^�[�[�ifructose-1,6-bisphosphatase�j
�@�t���N�g�[�X-1,6-�r�X�z�X�t�@�^�[�[�i�ʖ��Afructose-1,6-diphosphatase�j�́A�זE���]���ŁA�t���N�g�[�X-1,6-�r�X�����_���A�t���N�g�[�X-6-�����_�ɕϊ�����y�f�i�z�X�z�t���N�g�L�i�[�[�̉I��H�j�B
�@�Ȃ��A�t���N�g�[�X-2,6-�r�X�����_�́AAMP���l�ɁA�t���N�g�[�X-1,6-�r�X�z�X�t�@�^�[�[�̊�����}�����A���V����}�����܂��B�t���N�g�[�X 2,6-�r�X�����_�́A�܂��A�z�X�z�t���N�g�L�i�[�[�iPFK�j�̊������������A�̑��ł����𑣐i�����܂��B
�@���̂悤�ɁA�t���N�g�[�X 2,6-�r�X�����_�̗ʂ������ƁA�n�ɐi�݁A�t���N�g�[�X 2,6-�r�X�����_�̗ʂ����Ȃ��ƁA���V���n�ɐi�݂܂��B
�@�t���N�g�[�X-1,6-�r�X�z�X�t�@�^�[�[����������ƁA���V�����s��ꂸ�A�����Ԃ���H��A�ʓ���O���Z���[���̓��^�ɂ��A�����Ȓጌ����A��Ӑ��A�V�h�[�V�X�𗈂����܂��B
�@�T�D�O���R�[�X-6-�z�X�t�@�^�[�[�iglucose-6-phosphatase�j
�@�O���R�[�X-6-�i�����_�j�z�X�t�@�^�[�[�́A�̑��Ɛt���̃~�N���\�[���ɂ̂ݑ��݂��A�O���R�[�X-6-�����_���A�O���R�[�X�ɕϊ�����y�f�i�w�L�\�L�i�[�[�̉I��H�j�B
�@���V���́A�O���R�[�X-6-�z�X�t�@�^�[�[��L����A�̑��Ɛt�玿�ł̂݁A�s��꓾�܂��B
�@���V���ɂ́A�זE���]���i�T�C�g�]���j�ɁANADH2+�����݂��邱�Ƃ��A�K�v�ł��i���S�j�B
�@�~�g�R���h���A������A�זE���]���ցANADH2+�̊Ҍ����ʁireducing equivalents�j��A����������́A�����S�_�A���n�i�����S�_-��-�P�g�O���^���_�A�����j�ɂ��s���܂��F�~�g�R���h���A���Ő������ꂽNADH2+�́A�I�L�T���|�_���A�����S�_�ɊҌ����܂��B�����S�_�́A�~�g�R���h���A�����������S�_�A���n��ʉ߂��āA�זE���]���i�~�g�R���h���A�O�j�ɗA������A�ĂсA�I�L�T���|�_�ɖ߂�܂��B���̍ہANAD+���ANADH2+�ɊҌ������̂ŁA���ʓI�ɁA�~�g�R���h���A�O�i�זE���]���j�ɁANADH2+���A������܂��B
�@�Ȃ��A���_���瓜�V������ۂɂ́A�זE���]���ŁA�s���r���_�����������ۂɁANADH2+����������܂��B
�@�܂��A�ʓ����瓜�V������ۂɂ́AATP�i�~�g�R���h���A�Ő�������܂��j�͕K�v�ł����ANADH2+�͕K�v�ł���܂���B
�@���V���ɕK�v��NADH2+�́A���b�_���~�g�R���h���A������-�_�������ہiFADH2�����������j��A��-�_���Ő��������A�Z�`��-CoA��TCA��H�ő�ӂ����ۂɁA��������A��������܂��i���T�j�B
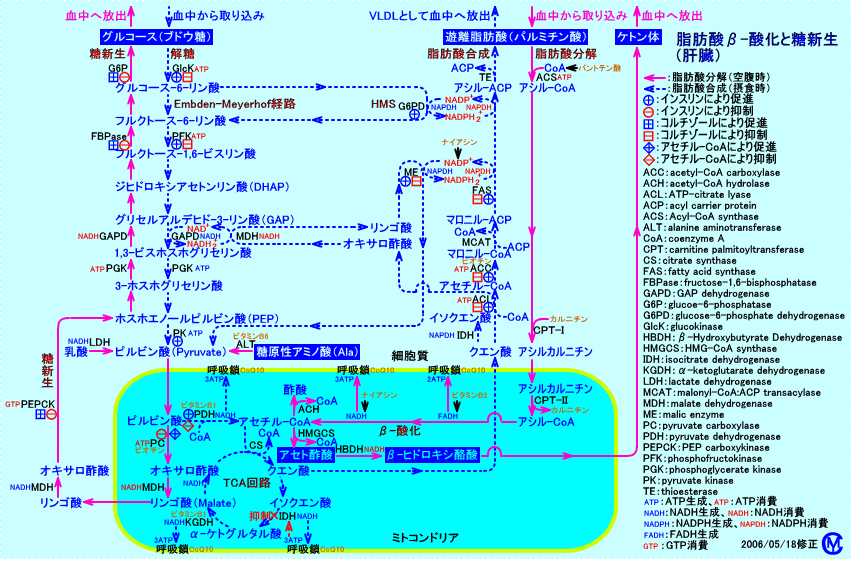
�@���V���ł́A�O���R�[�X�i�u�h�E���j�́A���_��s���r���_�i�ꕔ�́A�A���j������U�������j����A��������܂��B
�@���b�_�́A�~�g�R���h���A���ŁA��-�_���ɂ��A�A�Z�`��-CoA�ɕ�������A���̍ہANADH2+��FADH2����������܂��B�A�Z�`��-CoA��TCA��H�ő�ӂ��ꊮ�S�ɕ�������i�̑��ł��P�g�����ɕϊ������j�ANADH2+�̓~�g�R���h���A�O�ɊҌ����ʂ��A�����ꓜ�V���ɗ��p����܂��B
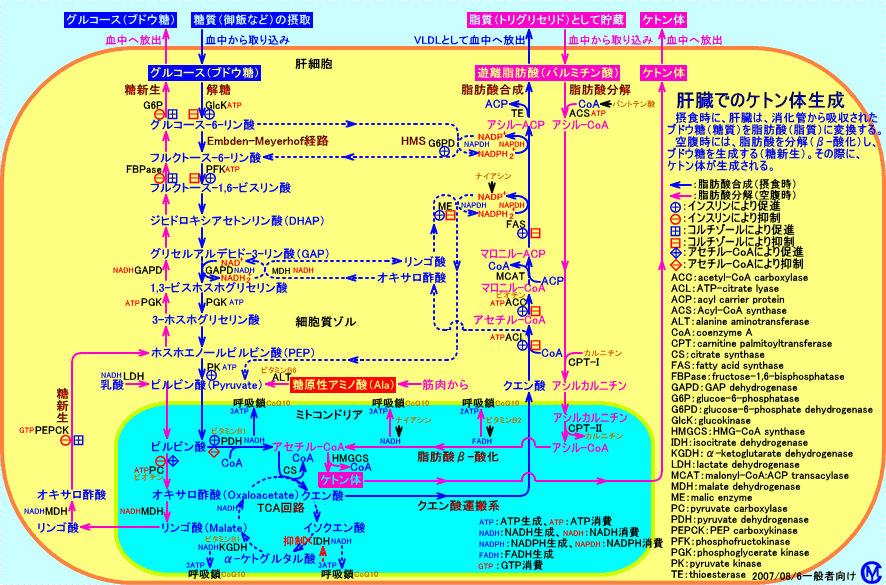
�@�����̑̂ɂ́A�A�Z�`��-CoA���A�I�L�T���|�_�ɕϊ������ӌo�H�́A����܂���B
�@�]���āA���b�_����́A���V���ŁA�u�h�E������������邱�Ƃ͂���܂���B
�@���b�_�́A���ꎩ�̂́A�O���R�[�X�ɁA�ϊ�����܂���B
�@�������A���b�_�̃�-�_���ɂ��A�זE���̃A�Z�`��-CoA�Z�x�ƁANADH/NAD+�����A��������ƁA���V�����A���i����܂��B
�@�]���āA���b�_�́A���ꎩ�̂́A�O���R�[�X�ɕϊ�����܂��A���V���ɕK�v��NADH2+���A��-�_����ATCA��H�ł̑�ӂŋ������A�܂��A���V���ɕK�v��ATP���ATCA��H�ł̑�ӂŋ������A���V���𑣐i�����A�O���R�[�X���������܂��B
�@���b�_�̃�-�_���Ɉُ킪���鎉�b�_�_���ُ�ǁiFAOD�j�ł́A���V������Q����A�Q�쓙�̐�H���ɁA��P�g�����ጌ���𗈂����܂��B����́A��H���ɁA���b�_�̃�-�_������Q����Ă���ƁA���b�_����A�Z�`��-CoA����������Ȃ��̂ŁATCA��H�ŁANADH2+���������ꂸ�A���V�����A�s���Ȃ����߂ƁA�l�����܂��B�]���āA���b�_�̃�-�_���Ő��������A�Z�`��-CoA�́A�^�����ɁA�ؓ��̃~�g�R���h���A�ŁANADH2+����ATP�����錴���ƂȂ邾���łȂ��A�̑��ł́ANADH2+���זE���ɋ������āA���V���̃G�l���M�[���ƂȂ�܂��i�P�g�����́A�]�̃G�l���M�[���ɂȂ�܂��j�B
�@�Ȃ��A���V���ɂ́ANADH2+�ȊO�ɁAATP�i�~�g�R���h���A�Ő��������j�AGTP���A�G�l���M�[���Ƃ��āA�K�v�ł��B
�@2�s���r���_�{4ATP�{2GTP�{2NADH2+�{6H2O���O���R�[�X�{4ADP�{2GDP�{6�����_�iPi�j�{2NAD+�{2H+
�@�Q�쓙����H���ɂ́A�ؓ��̒`��������������A�������A�~�m�_����A�s���r���_���I�L�T���|�_����������A���V���ɂ���āA�O���R�[�X�i�u�h�E���j���A��������܂��
�@�C���X�����́A�̑��ŁA�O���R�[�Q��������}�����A�A�~�m�_�A���_�A�O���Z���[���i�O���Z�����j������̓��V����}�����A�O���R�[�X�̕��o��}�����܂��B���̌��ʁA�̑��ɁA�O���R�[�Q�����A��������܂��B
�@�C���X�����́A���n�̗����y�f�i���ߍy�f�j�ł���A�O���R�L�i�[�[�A�z�X�z�t���N�g�L�i�[�[�A�s���r���_�L�i�[�[�A�s���r���_�f�q�h���L�i�[�[��U���A���邢�́A�����������܂��B�܂��APEPCK�A�O���R�[�X-6-�z�X�t�@�^�[�[�iglucose-6-phosphatase �j�̓]�ʂ�}�����A���V����}�����܂��B
�@�C���X�����́A�̑��ł̃O���R�[�Q��������}�����A���V�������}������̂ŁA�lj��C���X�������傪�ቺ���铜�A�a�ł́A�̑��ł̃O���R�[�Q�������ⓜ�V�������i���A���ɍ���������N���܂��B
�@��Ԃ��A�]�A�Ԍ����A�S�ؓ��ł́A�����ȓ���ӂ��s���Ă��܂��B
�@����́A�̑��ɂ́A�O���R�[�Q������������Ă��āA�̑����A�O���R�[�Q����������A���V�������āA�O���R�[�X�i�u�h�E���j�������ɋ������邩��A�\�ł��F���������O���R�[�X�i�u�h�E���j�́A��75���̓O���R�[�Q�������ɂ��A��25���͓��V���ɂ��A�Y������܂��B���V���́A���i�Œ`��������������Đ��������A�~�m�_�i�A���j�����j��A���b�g�D���������b����������Đ��������O���Z���[����A����������ɂ�萶���������_��s���r���_���A�ޗ��ɗp�����܂��B
�@�Ȃ��A�ؓ��ɂ��A�O���R�[�Q������������Ă��܂����A�ؓ��̃O���R�[�Q�����������ꐶ�������O���R�[�X�́A��ɋؐ��ۂ̊����ɗ��p����A�����ێ��ɂ͊�^���܂���B
�@�]�́A1���ԓ������4g�i���Î��ɂ͖�3g�j���O���R�[�X������A�Ԍ����́A1���ԓ������2g�̃O���R�[�X�������ƌ����܂��B
�@���N�l�ł́A���V���ɂ��A��ΓI�ɕK�v��6g/���Ԃ̃O���R�[�X�����܂��B
�@�����ł́A�A�Z�`��-CoA���A�I�L�T���|�_�ɕϊ�����y�f���A���݂��܂���B�]���āA��-�_���ŃA�Z�`��-CoA�ɕ�������鎉�b�_�́A�O���R�[�X�O��̂Ƃ��āA���V���Ɏg�p����܂���B�������A���b�_����-�_�������ۂɐ��������NADH2+��A���b�_�̃�-�_���ɂ�萶�������A�Z�`��-CoA��TCA��H�ő�ӂ���Đ��������NADH2+��ANADH2+�������ċz���Ő��������ATP�́A���V���ɃG�l���M�[���Ƃ��āA���p����܂��B���������Ӗ��ŁA���b�_�̃G�l���M�[�́A�̑��ł̓��V���ɕK�v�ł��B
�@���܂�
�@���̂P�F�A�X�s�����ƒጌ��
�@�A�X�s�����̑�ӎY�����T���`���_�́A���_�A�s���r���_����̓��V�����A���������܂��B
�@���̋@���́A���C�nj�Q�̔��Nj@���Ƃ��֘A����Ǝv���܂����A�~�g�R���h���A�ɂ́APTP�ƌĂ�錊�\��������܂����A�T���`���_�ɂ́APTP���J���������p�����邱�Ƃ��A�m���Ă��܂��B�T���`���_�ɂ��APTP���J���ƁA�~�g�R���h���A���i�}�g���b�N�X�j�̃v���g�������A�זE���]���ɒʉ߂��Ă��܂��A���d�ʂ��ቺ���āA�~�g�R���h���A����NADH2+���������Ă��܂��̂ŁA�זE���]���ł̓��V�����A�������A�ጌ���𗈂����ƁA�l�����܂��B
�@�Ȃ��APGE2��IL-1���́A�O���R�[�X�i�u�h�E���j�ɂ���C���X����������A�}�����܂��BCOX-2�ɂ��Y�����ꂽPGE2�́AEP3��e������āA�A�f�j���_�V�N���[�[�iAC�j��}������̂ŁAcAMP���������A�C���X�������傪�A�}������܂��BIL-1���́ANF-��B�̔�������āACOX-2����������iPGE2�̎Y������������j�AEP3��e�̂�mRNA��������̂ŁA�C���X�������傪�A�}������܂��B
�@�T���`���_�́AIL-1���ɂ��ANF-��B�̔�����}�����ACOX-2��AEP3��e�́iEP3��e�́j��mRNA�̔�����W���āAPGE2�ɂ��C���X��������}����p��}������̂ŁA�C���X�������傪�A�������A�ጌ���ɂȂ邱�Ƃ�����܂��B
�@�Ȃ��A�A�X�s�����́AIL-1���ɂ��ANF-��B�̔�����}�����Ȃ��̂ŁA�C���X��������ɉe������̂́A�A�X�s�����łȂ��A�T���`���_�ƍl�����܂��B
�@���̂悤�ɁA�T���`���_�́ANADH2+�����������ē��V����}��������APGE2�̎Y�������������ăC���X��������𑣐i������̂ŁA�A�X�s�����p����ƁA�ጌ���𗈂������Ƃ�����܂��B
�@�Ȃ��A�A�X�s�����ȊO��NSAIDs�i�A�Z�g�A�~�m�t�F�����j���APGE2�̎Y�������������ăC���X��������𑣐i�����邱�Ƃɂ���āA�ጌ���𗈂��������ꂪ����܂��B�@
�@���̂Q�F��䍓����ł̓��_��v���s�I���_����̓��V��
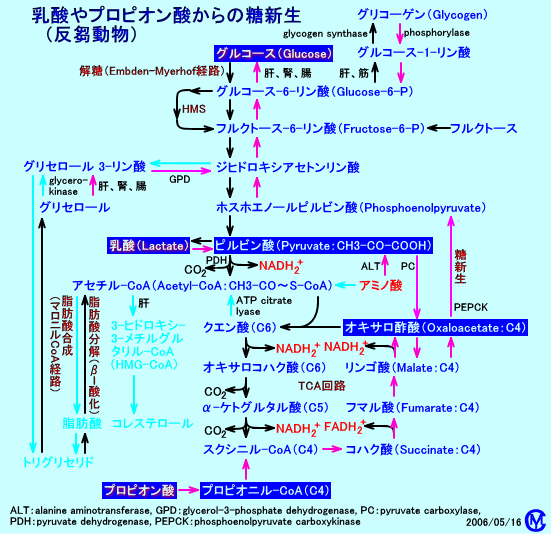
�@��䍓����i�E�V�A�q�c�W�A�L�����A�V�J�A���N�_���j�ł́A���[�����i���݁j���ŁA�������ɂ��A���_��v���s�I���_�i�Z�����b�_�j���Y������܂��B
�@���_�́A�s���r���_�ɕϊ�����A���V���ɗ��p����܂��B
�@�܂��A�v���s�I���_�́A�v���s�I�j��-CoA�ɕϊ�����A����ɁATCA��H�̃X�N�V�j��-CoA�ɕϊ�����A�ŏI�I�ɁA�I�L�T���|�_�ɕϊ�����A���V���ɗ��p����܂��B
�@���̂悤�ɁA��䍓����ł́A���[�����i���݁j���ŁA�������ɂ��Y�����ꂽ���_��v���s�I���_�́A�w�ǑS�Ă��A���V���ɂ��A�O���R�[�X�i�u�h�E���j�ɕϊ�����܂��B
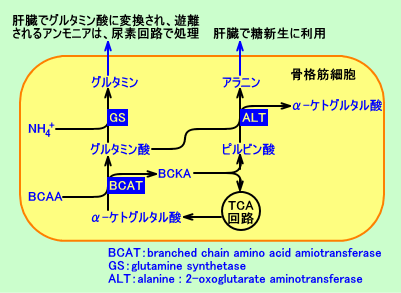
�@���P�F���i�ŁA�^�����ɁABCAA���琶��������O���^�~���_�́AALT�iGPT)�ɂ��A�s���r���_�ɁA�A�~�m���]�ڂ��A�������A�~�m�_�ł���A�A���j������������܂��B�A���j���́A���t�����̑��ɗA������AALT�iGPT)�ɂ��A�s���r���_�ɖ߂�A�O���R�[�X�ɓ��V������܂��B���V�����ꂽ�O���R�[�X�́A�̑�������o����A���t�������i�ɗA������A���p����܂��i�O���R�[�X�E�A���j���T�C�N���j�BBCAA�̃��C�V���iLeu�j�́A�P�g�����A�~�m�_�ł����A���i�ł́ABCAT�ɂ��A��-�P�g�O���^���_�ɃA�~�m���]�ڂ��āA�O���^�~���_����������A���V���Ɋ֗^����Ǝv���܂��B
�@���̂悤�ɁABCAA�́A�^�������ɁA���i�ňى�����A���������O���^�~���_����A�A���j������������A�̑��ł̓��V�����A���i������ƍl�����܂��B
�@�������ɍۂ��āA���̂́A�]�̔��B���A�ؓ���A�����̔��B���A�D�悵�Ă��܂��i����ɂ��A�h�{�̗D�揇�����قȂ�j�B�ؓ��́A�O���R�[�Q����A���V���̌����ɂȂ铜�����A�~�m�_��A�~�l�������A�h�{�f�̒����ɂƂ��Ă̖������A�S���Ă��܂��B
�@�A���j���Ɋւ��ẮA�����g�D�i���i�ؓ��j�ŁA��Ӂi�j�ɂ�萶�������s���r���_�ƁA�O���^�~���_�̂悤�ȃ�-�A�~�m�_�Ƃ��AALT�iGPT)�ɂ��A�~�m��]�ڔ������āA�A���j������������܂��B���̖����g�D�̃A���j���́A����ɁA���t�����A�̑��ɗA������A�̑��ŁA��-�P�g�O���^���_�ƁAALT�iGPT)�ɂ��A�~�m��]�ڔ������āA�s���r���_�ɕϊ�����A���V���ɗ��p����܂��B
�@�A�X�p���M���_�Ɋւ��ẮA�A�X�p���M���_�́A�A�f��H�ɉ����āA�t�}���_����S�_���o�ăI�L�T���|�_�ɕϊ�����A���V���ɗ��p����܂��B
�@1���A�Œ�50g�̃O���R�[�X�𓊗^����ƁA���V���̂��߂ɁA�`���������i�ى��j����邱�Ƃ��A�}�������ƌ����Ă��܂��i�̒`���ى��}�����ʁFprotein sparing effect�j�B�_�H�ȂǂŃO���R�[�X�i�u�h�E���j��⋋����ƁA��H���Ă��Ă��A�̏d���������Ȃ��Ȃ�܂��B
�@���Q�F���_�́A�s���r���_����LDH�̍�p�ɂ��A��������܂��B
�@���_�́A��ɁA���i��Ԍ����ŁA��������Ă��܂��B
�@���i�ŁA���C�I�Ő������ꂽ���_�́A���t�����̑��ɗA������ALDH�ɂ��A�s���r���_�ɕϊ�����A�O���R�[�X�ɓ��V������܂��B���V�����ꂽ�O���R�[�X�́A�̑�������o����A���t�������i�ɗA������A���p����܂��iCori�̃T�C�N���F�R����H�j�B���i�؈ȊO�ɁA�Ԍ����ȂǂŐ����������_���A�̑��ŁA�O���R�[�X�ɓ��V������܂��B
�@�̑���t���ł̓��V������Q�����ƁA�s���r���_����_���A���t���ɑ������܂��B
�@���V���ɍۂ��āA�i�~�g�R���h���A���́j�s���r���_�́A�I�L�T���|�_���o�āA�����S�_�ƂȂ��āA�~�g�R���h���A�O�ɗA������܂����A�i�~�g�R���h���A���́j���_�́A�����S�_�Ƃ��Ăł͂Ȃ��A�A�X�p���M���_�ƂȂ��āA�~�g�R���h���A�O�ɗA������܂��B
�@���R�F�q�g�ł́APEPCK�́A�~�g�R���h���A���ɂ��A�זE���]���i�T�C�g�]���j�ɂ��A���݂���BPEPCK�́A������ɂ���ẮA�~�g�R���h���A���ɂ̂ݑ��݂�����A�זE���]���ɂ̂ݑ��݂����肷��B
�@���S�F�A�~�m�_�i�������A�~�m�_�j�̒Y�f���i�A�s���r���_�A���_�ATCA��H�̒��ԑ̂���A�I�L�T���|�_���o�R���āA���V������ۂɂ́A1,3-�r�X�z�X�z�O���Z�����_�i1,3-bisphosphoglycerate�F1,3-BPG�j���A�O���Z���A���f�q�h-3-�����_�iglyceraldehyde-3-phosphate�FGAP�j�ɕϊ������ׂɁANADH2+���K�v�ł��B�ʓ���O���Z���[������A���V������ۂɂ́A1,3-BPG����Ȃ��ŁA�W�q�h���L�V�A�Z�g�������_�iDHAP�j�ɕϊ������̂ŁANADH2+��GTP�́A�K�v�ł���܂��AATP�́A�K�v�ł��B
�@���T�F���b�_�̕����i��-�_���j�́A�_�f��K�v�Ƃ��܂��B
�@���b�_�̔M�����́A���̉h�{�f��荂���A�Ⴆ�A�p���~�`���_���A��-�_�������ƁA�P�R�T���q��ATP����������܂��F�p���~�`���_�iC16:0�j���A��-�_���łP������A�P�̃A�Z�`��-CoA�����������ۂɁA�P��FADH2�ƂP��NADH2+�Ƃ������܂��B�~�g�R���h���A���ċz���ŁAFADH2��NADH2+����A���ꂼ��A�Q�A�y�сA�R��ATP����������܂��i�v�T��ATP����������܂��j�B�p���~�`���_�́A�A�Z�`��-CoA�ɕ���������-�_�����V��J��Ԃ��̂ŁA�v�R�T��ATP����������܂��i�V��̃T�C�N�����̃�-�_���ɂ��A�W�̃A�Z�`��-CoA����������܂��j�B�A�Z�`��-CoA���ATCA��H�ő�ӂ����ƁA�P�P��ATP�ƂP��GTP����������܂��B�]���āA��-�_����TCA��H�ŁA�v�R�T�{�i�P�Q�~�W�j���P�R�P��ATP����������܂��B�������A�p���~�`���_�iC16:0�j���A��-�_������鏉���̒i�K�ŁAThiokinase�iACS�j�ɂ��A�A�V��-CoA�iC15-CO-CoA�j�ɕω�������̂ɁA�P��ATP�������AMP�ɂȂ�i�����A2ATP������j�̂ŁA���������A�P�Q�X��ATP����������܂��i�������A�̑��ł́A�p���~�`���_�́A��-�_�����ꂽ��ATCA��H�ɓ��炸�A�P�g���̂̃A�Z�g�|�_�ɂȂ�̂ŁA�R�T�|�Q���R�R��ATP�����A��������܂���j�B
�@�]���āA�O���R�[�X�P���q�i�Pmol�j����R�W��ATP�i�O���R�[�X�P�O�Og����Q�P��ATP�j����������A�p���~�`���_�P���q�i�Pmol�j����P�Q�X��ATP�i�p���~�`���_�P�O�Og����T�O��ATP�j����������܂��i���b�_�̕����A�u�h�E�����A�G�l���M�[�͉��������j�B
�@�Q�l����
�@�E��؍h��A���F�z�[�g�������w�@��R�Łi�������w���l�A2005�N�A��3���j�D
�@�E���H�[�g�����w�i�������w���l�A2003�N�A��S���j�D
�@�E�n�[�p�[�E�����w�i�ۑP������Д��s�A1975�N�j�D
�@�E�e�r�����F�̂ɂ����铜���ߋ@�\�ɂ��ā@���{�Ύ��V��@No.4184�i2004�N7��3���j�A21-30�ŁD
�@�E�c��M�v�F���炾�̓�������݂��ӂ̉h�{�w�@�^�J���o�C�I������Ёi2003�N�j�D
�@�b�g�b�v�y�[�W�b�����ƌ����̊W�b�~�j��w�m���b�����w�̒m���b��w�̘b���b�����Ȏ����b�����̕s�v�c�b�����N�W�b